Remédios sem autorização são apreendidos na BR-116 em Vitória da Conquista
Substâncias sem liberação da Anvisa estavam em ônibus interestadual
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Polícia Rodoviária Federal Bahia
A Polícia Rodoviária Federal (PRF) apreendeu medicamentos de uso proibido e sem documentação durante fiscalização na BR-116, em Vitória da Conquista, no sudoeste da Bahia. A abordagem ocorreu na tarde de quarta-feira (22), no km 830, em um ônibus interestadual que fazia a linha entre São Paulo e Garanhuns.Durante a inspeção de encomendas, os agentes encontraram 36 seringas de retatrutida, substância ainda em fase experimental e sem autorização da Agência Nacional de Vigilância Sanitária (Anvisa) para uso no país. Também foram localizados frascos de tirzepatida, conhecida comercialmente como Mounjaro, sem comprovação de origem ou autorização para transporte.O material foi apreendido e encaminhado à Receita Federal em Vitória da Conquista. Segundo a PRF, a ação faz parte de operações de combate ao transporte irregular de produtos nas rodovias federais.
Anvisa autoriza uso do Mounjaro para adolescentes com diabetes tipo 2
Medida ocorre em meio ao aumento de casos na população jovem; estudos indicam melhora no controle glicêmico
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)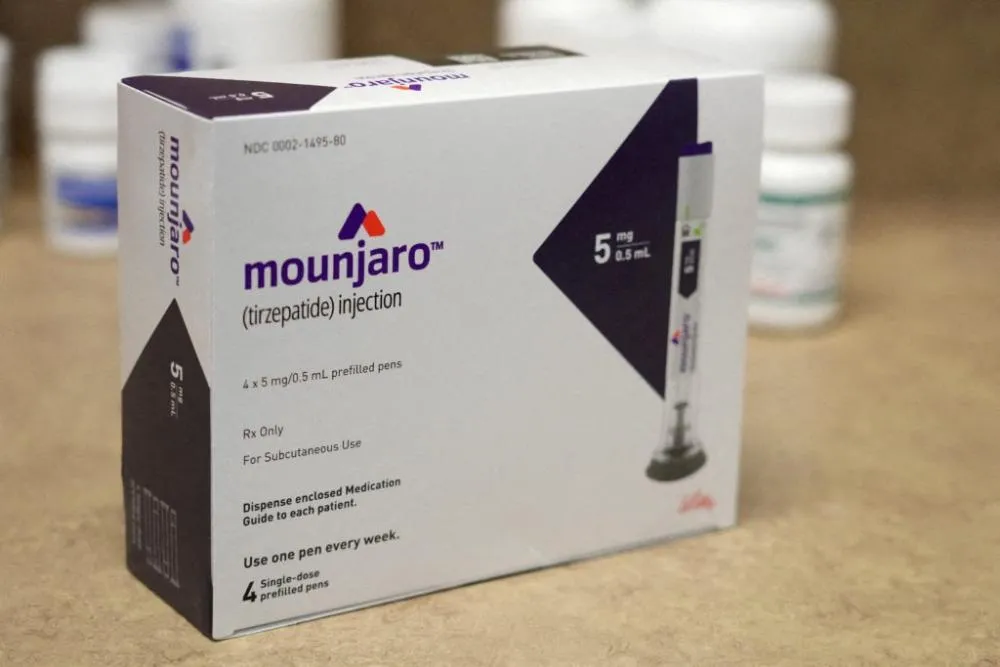
Foto: Reprodução
A Agência Nacional de Vigilância Sanitária autorizou o uso do medicamento Mounjaro para o tratamento de diabetes tipo 2 em pacientes com idade entre 10 e 17 anos.A decisão amplia a indicação do fármaco, que até então era destinado apenas a adultos, e ocorre em meio ao aumento de diagnósticos da doença entre adolescentes.O medicamento atua no controle dos níveis de glicose no sangue e também contribui para a redução do peso corporal, fatores considerados centrais no tratamento do diabetes tipo 2.Dados clínicos, como os do estudo SURPASS-PEDS, publicados pela revista científica The Lancet, indicam melhora significativa no controle glicêmico e no índice de massa corporal em poucas semanas de uso.Especialistas apontam que o avanço do sobrepeso e da obesidade entre jovens tem relação direta com o crescimento dos casos. A Sociedade Brasileira de Diabetes reforça a importância do acompanhamento médico no tratamento.Os efeitos adversos mais comuns relatados são gastrointestinais, como náusea e diarreia, geralmente considerados leves e transitórios. Estudos também indicam manutenção dos benefícios ao longo do tempo.
Anvisa quer endurecer regras para manipulação de medicamentos de GLP-1
Medida prevê regras técnicas para produção e controle de qualidade; agência também intensifica combate ao mercado ilegal
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
A Agência Nacional de Vigilância Sanitária (Anvisa) deve analisar, no próximo dia 29, uma proposta de instrução normativa que estabelece regras para a manipulação de medicamentos da classe dos agonistas do receptor GLP-1, conhecidos como canetas emagrecedoras. A medida integra um plano de ação anunciado pela agência neste mês, que reúne iniciativas regulatórias e de fiscalização voltadas ao controle desse tipo de produto.A proposta prevê a definição de critérios técnicos para importação, qualificação de fornecedores e realização de testes de controle de qualidade, além de regras para armazenamento e transporte de insumos farmacêuticos ativos. Medicamentos como os que utilizam semaglutida, tirzepatida e liraglutida ganharam popularidade recente, o que, segundo a agência, ampliou o mercado ilegal. Atualmente, a venda desses produtos exige receita médica retida. Anvisa afirma que tem intensificado ações para coibir a comercialização irregular, incluindo versões manipuladas sem autorização. FISCALIZAÇÃO E MEDIDAs: Nesta semana, a agência instituiu dois grupos de trabalho para apoiar o controle sanitário e ampliar a segurança no uso desses medicamentos. Um dos grupos reúne representantes do Conselho Federal de Farmácia, Conselho Federal de Medicina e Conselho Federal de Odontologia.O outro será responsável por acompanhar a execução das ações e propor ajustes regulatórios. Também foi firmada uma carta de intenção entre a Anvisa e os conselhos profissionais para promover o uso racional e seguro dos medicamentos.PRODUTOS IRREGULARES: Na quarta-feira (15), a Anvisa determinou a apreensão dos produtos Gluconex e Tirzedral, comercializados como canetas emagrecedoras sem registro no país.Segundo o órgão, os itens não possuem autorização e não há garantia de qualidade ou composição, o que representa risco à saúde. CONTRABANDO: Na segunda-feira (13), uma ação da Polícia Civil do Estado do Rio de Janeiro interceptou, em Duque de Caxias, um ônibus vindo do Paraguai com medicamentos ilegais. Dois suspeitos foram presos em flagrante com anabolizantes e cerca de mil frascos de canetas emagrecedoras contendo tirzepatida.
Anvisa proíbe canetas emagrecedoras vendidas na internet
Venda, fabricação, importação e uso de produtos sem registro foram totalmente proibidos pela agência.
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
A Agência Nacional de Vigilância Sanitária (Anvisa) proibiu, nesta quarta-feira (21), a comercialização, fabricação, distribuição, importação, divulgação e o uso de medicamentos à base de tirzepatida das marcas Synedica e TG, além de produtos que contenham retatrutida, de todas as marcas e lotes.Os itens são conhecidos popularmente como “canetas emagrecedoras do Paraguai” e vinham sendo comercializados, principalmente, por meio de redes sociais, como o Instagram.De acordo com a Anvisa, os produtos são fabricados por empresas desconhecidas e não possuem qualquer tipo de registro, notificação ou cadastro junto ao órgão regulador, o que torna a comercialização irregular em todo o território nacional.Em nota, a agência alertou que, por se tratarem de medicamentos de origem incerta, não há garantia sobre a composição, qualidade, eficácia ou segurança. Por esse motivo, a Anvisa afirmou que os produtos não devem ser utilizados “em nenhuma hipótese”.“A ausência de controle sanitário impede qualquer confirmação sobre o que, de fato, está sendo aplicado no organismo do consumidor”, destacou o órgão no comunicado.A resolução que determina a proibição foi publicada no Diário Oficial da União nesta quarta-feira e já está em vigor. O descumprimento da medida pode gerar sanções administrativas, incluindo multas e apreensão dos produtos, além de responsabilização civil e criminal dos envolvidos.A Anvisa reforça que medicamentos só devem ser adquiridos em estabelecimentos regularizados e com prescrição médica, quando exigida, e orienta a população a denunciar a venda de produtos irregulares pelos canais oficiais do órgão.
Anvisa aprova lenacapavir como nova estratégia de PrEP no país e com quase 100% de eficácia
Remédio depende agora da definição de preço e de avaliação para possível incorporação ao SUS.
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta segunda-feira (12) o registro do lenacapavir para uso como profilaxia pré-exposição (PrEP), com a finalidade de diminuir o risco de infecção pelo HIV-1 por transmissão sexual no Brasil. A indicação é voltada a adultos e adolescentes a partir de 12 anos, com peso mínimo de 35 quilos, que apresentem risco de exposição ao vírus. Antes do início do tratamento, é obrigatória a realização de teste com resultado negativo para HIV-1.Apesar da autorização sanitária, o medicamento ainda não pode ser comercializado. A liberação depende da definição do preço máximo pela Câmara de Regulação do Mercado de Medicamentos (CMED). A eventual oferta pelo Sistema Único de Saúde (SUS) será analisada pela Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec) e pelo Ministério da Saúde. O lenacapavir atua em diferentes etapas do ciclo de vida do HIV-1, inibindo a função do capsídeo viral e impedindo a replicação do vírus. Com isso, o agente infeccioso perde a capacidade de sustentar a transcrição reversa, processo essencial para a infecção das células humanas.O medicamento possui duas apresentações: uma injeção subcutânea aplicada a cada seis meses e um comprimido oral utilizado no início do esquema terapêutico. A proposta é reduzir a dependência do uso diário de medicamentos, ampliando a adesão ao tratamento preventivo. Segundo a farmacêutica Gilead Sciences Brasil, o registro também contempla o uso do lenacapavir no tratamento de pacientes multiexperimentados (HTE), que vivem com HIV-1 e apresentam resistência a múltiplas classes de antirretrovirais.A PrEP é considerada uma das principais estratégias de prevenção ao HIV. Ela consiste no uso de antirretrovirais por pessoas não infectadas, mas em situação de maior vulnerabilidade, com comprovada redução do risco de transmissão do vírus. No Brasil, a PrEP está disponível gratuitamente pelo SUS desde 2018, na forma de comprimido diário, com a combinação de tenofovir disoproxil e emtricitabina. Embora eficaz, o modelo exige adesão contínua e acompanhamento periódico em unidades de saúde.O lenacapavir já recebeu aprovação da Food and Drug Administration (FDA), nos Estados Unidos, tanto para uso como PrEP injetável semestral quanto para tratamento de pacientes HTE. Na União Europeia, foi autorizado sob o nome comercial Yeytuo, e outros países seguem com processos regulatórios em andamento. Em julho de 2025, a Organização Mundial da Saúde (OMS) passou a recomendar o lenacapavir como alternativa adicional para a PrEP, classificando-o como a opção mais promissora depois de uma vacina contra o HIV.A PrEP integra a chamada prevenção combinada, que reúne diferentes estratégias de controle da infecção, como testagem regular para HIV, uso de preservativos, tratamento antirretroviral para pessoas vivendo com o vírus, profilaxia pós-exposição (PEP) e cuidados específicos no acompanhamento de gestantes soropositivas. Com o aval da Anvisa, o lenacapavir passa a compor o conjunto de tecnologias disponíveis no país para o enfrentamento do HIV, ampliando as possibilidades de prevenção e fortalecendo as políticas públicas de controle da infecção.Ensaios clínicos apresentados à agência reguladora indicaram 100% de eficácia na redução da incidência de HIV-1 entre mulheres cisgênero. Os estudos também apontaram redução de 96% em comparação à incidência de base e desempenho 89% superior ao da PrEP oral diária.
Anvisa libera medicamento para fase inicial do Alzheimer
Leqembi é indicado para pacientes com demência leve e atua na redução de placas no cérebro.
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso do medicamento Leqembi para o tratamento de pacientes diagnosticados na fase inicial da doença de Alzheimer. A autorização foi publicada no Diário Oficial da União no dia 22 do mês passado. O remédio tem como princípio ativo o anticorpo monoclonal lecanemabe e é indicado para retardar o declínio cognitivo em pessoas que já apresentam demência leve associada à doença. O produto é administrado por infusão intravenosa após diluição.De acordo com o registro da Anvisa, o lecanemabe atua reduzindo o acúmulo de placas beta-amiloides no cérebro, uma das principais características patológicas do Alzheimer. Essas placas estão associadas à progressão da doença e à perda das funções cognitivas. A eficácia clínica do medicamento foi avaliada em um estudo principal que envolveu 1.795 pacientes com Alzheimer em estágio inicial, todos com presença comprovada de placas beta-amiloides. Os participantes receberam o Leqembi ou placebo ao longo do período de análise.Segundo a Anvisa, a principal medida de eficácia foi a evolução dos sintomas após 18 meses de tratamento, avaliada por meio da escala CDR-SB (Clinical Dementia Rating – Sum of Boxes), utilizada para medir a gravidade da demência e o impacto do comprometimento cognitivo na rotina do paciente. Os resultados indicaram que, em um subgrupo de 1.521 participantes, os pacientes tratados com o novo medicamento apresentaram progressão mais lenta da doença, com aumento menor na pontuação da escala CDR-SB em comparação aos que receberam placebo.
Anvisa suspende lotes do detergente Ypê por risco de contaminação
Empresa afirmou que já iniciou o recolhimento dos lotes defeituosos
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
- A Agência Nacional de Vigilância Sanitária (Anvisa) ordenou o recolhimento de lotes dos detergentes Ypê após a fabricante ter identificado, em análise, um "potencial risco de contaminação microbiológica". A resolução foi publicada na edição de terça-feira (7) do Diário Oficial da União. A Química Amparo, fabricante do produto, afirmou em nota que identificou mudanças no odor tradicional do produto de limpeza, sem potencial risco à saúde dos consumidores e que o recolhimento dos lotes dos detergentes contaminados já foram iniciados. A resolução Anvisa também determinou a suspensão de todas unidades produzidas de julho a dezembro de 2022, que tenham o lote com final 1 e 3. As linhas de detergentes afetadas foram as de limão, maçã, neutro, capim limão, coco e clear care. Confira os lotes afetados: Versão Ypê Clear Care - 172051, 179054, 184054, 185054, 186054, 228054, 233011, 234011, 235011, 236011, 242054, 253011, 255011, 267051, 269051, 270051, 278011, 279011, 280011, 281011, 282011, 283011, 302051, 303051, 304051, 314011, 315011, 316011 e 318011. Versão Ypê Coco - 029016, 030016, 036016, 038016, 057016, 058016, 148051, 149051, 151051, 212044, 213051, 215051, 216051, 217051, 218051, 219051, 220051, 221051, 228054, 232051, 233051, 236051, 238051, 243044, 248051, 249051, 256051, 257051, 258051, 272051, 273051, 274051, 275051, 276051, 277051, 284051, 286051, 288051, 289051, 290051, 291051, 298051, 299051, 300051, 301051, 317016, 331051, 333051, 33405, 031016, 188031, 225081, 226081, 227081, 239081, 270031, 281031, 282031, 283031, 295031, 323016, 324016, 327031, 328031, 329031 e 330031. Versão Ypê Capim Limão - 225031, 226031, 242081, 314031, 323081, 325081, 060016, 173081, 174081, 175081, 176081, 177081, 178081, 223011, 224011, 239051, 240051, 242051, 271081, 272081, 273081, 299011, 300011, 302011, 303011, 326051, 327051, 336016, 337016, 338016, 346016 e 347016. Versão Ypê Limão - 031016, 040016, 041016, 042016, 043016, 127011, 129011, 130011, 134081, 135081, 136081, 137081, 138081, 148011, 149011, 150011, 218011, 219011, 310011, 311011, 319016, 332016, 339016, 347016, 053016, 054016, 141031, 221081, 222081, 223081, 227081, 228081, 229081, 279081, 280081, 288031, 315031 e 325016. Versão Ypê Maçã - 010016, 011016, 012016, 026016, 028016, 029016, 054016, 131011, 132011, 134011, 142011, 173011, 174011, 187011, 188011, 189011, 193011, 194011, 195011, 200051, 213011, 220011, 221011, 228011, 229011, 230011, 241011, 242011, 248081, 249081, 256011, 257011, 262011, 263011, 264011, 265011, 266011, 278061, 279061, 280061, 281061, 282061, 283051, 292011, 293011, 295011, 311011, 312011, 313011, 313061, 327011, 327016, 328011, 328016, 329011, 330011, 357016, 046016, 047016, 185081, 186081, 191081, 192081, 204101, 223081, 224081, 232081, 234081, 268031, 269031, 309031 e 310031. Versão Ypê Neutro - 019056, 020056, 037056, 038056, 039056, 054056, 055056, 173001, 174001, 186064, 188001, 211001, 212001, 225001, 226001, 228001, 228064, 237001, 239001, 272056, 320001, 321001, 322001, 324056, 325001, 325056, 326001, 326056, 327001, 331056, 336056, 338056, 356056, 236001, 016016, 017016, 024016, 025016, 026016, 038016, 039016, 040016, 172081, 172151, 173151, 174151, 175151, 176151, 177151, 178151, 188151, 207151, 208151, 209151, 210151, 211081, 212081, 225011, 226011, 227011, 228151, 229151, 230151, 232151, 233151, 234051, 234151, 235051.,235151, 236151, 239011, 241151, 279151, 282151, 283151, 317151, 318016, 318151, 321011, 322011, 325151, 326151, 327151, 328151, 333016, 342016, 346016, 349016, 048016, 049016, 050016, 051016, 176031, 177031, 207031, 208031, 227031, 229031, 236031, 237031, 238031, 282081, 316031, 317031, 318031, 319031, 323031, 325031, 326016, 327031, 353016, 355016, 052016, 171031, 173031, 174031, 209031, 230031, 232031, 233031, 234031, 235031, 239031 e 327016.
Venda de álcool líquido em supermercados volta a ser proibido pela Anvisa
O produto é considerado perigoso por ser altamente inflamável; a versão em gel segue liberada
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
- Supermercados e demais estabelecimentos estão proibidos de seguir com a venda de álcool líquido 70% segundo a Agência Nacional de Vigilância Sanitária (Anvisa). O órgão havia liberado a comercialização do produto até o dia 31 de dezembro de 2023, principalmente, devido à pandemia de Covid-19, para diminuir o contágio pelo vírus. Desde dezembro, apenas os estoques permitidos pela RDC Nº 766 estão sendo comercializados pelos estabelecimentos, que deveriam ter sido encerrados desde o sábado (29). A informação foi divulgada pelo blog Samanta Sallum, do jornal Correio Braziliense. Farmácias também não podem oferecer o produto. Apenas a versão em gel estão liberadas, sendo a mais segura de acordo com a Sociedade Brasileira de Queimaduras (SBQ), pois evita que seja derramada muitas quantidades, que podem causar queimaduras no corpo e acidente doméstico, onde as crianças são as principais vítimas.
Anvisa renova autorização de vacinas e medicamentos de uso emergencial
Para que sejam fabricados, produtos precisam de registro definitivo
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) publicou resolução que permite a utilização de medicamentos e vacinas autorizados para uso emergencial durante a pandemia de covid-19. Em nota, a agência destacou que, com o fim da emergência de saúde pública de importância nacional, a norma que estabelecia regras para concessão e manutenção das autorizações de uso emergencial perdeu a vigência. Comercialização - “Para que medicamentos e vacinas aprovados por meio dessas autorizações ainda possam ser utilizados, a Anvisa publicou a nova norma, permitindo o uso, a distribuição e a comercialização desses produtos, desde que tenham sido fabricados até o último dia 21 de maio”, esclarece a decisão. A nova resolução reconhece que os medicamentos e as vacinas mantêm sua eficácia e segurança e seguem com avaliação positiva na relação benefícios x riscos. Confira a lista abaixo: vacina Comirnaty bivalente BA.1; vacina Comirnaty bivalente BA.4/BA.5; vacina CoronaVac; medicamento Sotrovimabe e Lagevrio (molnupiravir); medicamento Paxlovid (nirmatrelvir + ritonavir). Ainda segundo a Anvisa, para que continuem a ser fabricados após 21 de maio, esses produtos precisam ter seu registro definitivo solicitado pelas empresas. “Até o momento, as vacinas CoronaVac e Comirnaty bivalente BA.4/BA.5, além do medicamento Paxlovid, já possuem pedido de registro em análise”, finalizou a Anvisa.
Anvisa aprova registro de nova vacina contra dengue
A aplicação é por via subcutânea e dividida em um esquema de duas doses, com intervalo de três meses entre as aplicações
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- Uma nova vacina contra a dengue foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa). O imunizante Qdenga é produzido pela empresa Takeda Pharma e é indicado para população entre 4 e 60 anos. De acordo com a Anvisa, o imunizante é composto por quatro diferentes sorotipos do vírus causador da doença, o que garante uma ampla proteção contra ela. A aplicação é por via subcutânea e dividida em um esquema de duas doses, com intervalo de três meses entre as aplicações. A vacina também foi avaliada e aprovada pela agência sanitária europeia (EMA). No Brasil, a concessão do registro pela Anvisa permite a comercialização do produto no país, desde que mantidas as condições aprovadas. A vacina, no entanto, seguirá sujeita ao monitoramento de eventos adversos por meio de ações de farmacovigilância sob a responsabilidade da própria empresa. Já existe no Brasil uma vacina aprovada contra a doença, a Dengvaxia. Mas ela só pode ser aplicada em quem já teve a doença. No ano passado, o país registrou mais de mil mortes por complicações da dengue.
Anvisa proíbe comercialização de pomadas para trançar e modelar cabelos
A agência tomou esta decisão após usuários de produtos capilares de diferentes marcas sofrerem com efeitos colaterais
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
Como medida de segurança, a Agência Nacional de Vigilância Sanitária (Anvisa) proibiu a comercialização de todas as pomadas para trançar, fixar e modelar cabelos. A decisão foi publicada na edição do Diário Oficial da União desta quinta-feira (9). A Anvisa tomou esta decisão após ficar ciente sobre vários casos de usuários destes produtos que sofreram com diversos efeitos colaterais nos olhos, entre eles: coceira, vermelhidão, inchaço e lacrimejamento intenso. Assim como queda de cabelo, fortes dores de cabeça e até perda temporária da visão. Vale ressaltar que a medida é provisória, para que enquanto esteja vigente, testes sejam realizados nestes produtos para apurar a ligação deles com os sintomas relatados por seus usuários. Além disso, a agência afirmou que as pomadas capilares compradas antes da decisão ter sido anunciada oficialmente pelo Diário Oficial também não devem ser utilizadas pela população.
Anvisa libera comercialização de autotestes de Covid-19
Os autotestes liberados são os de antígenos - feitos a partir da coleta do material no fundo da boca e do nariz e busca sinais de anticorpos ativos, gerados pelo corpo após a infecção
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)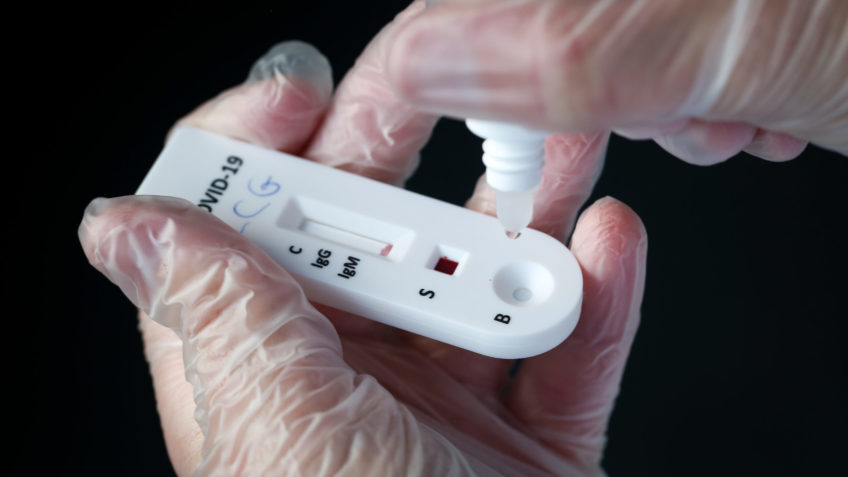
Foto: Reprodução
- A Agência Nacional de Vigilância Sanitária (Anvisa) liberou, nesta sexta-feira (28), a venda de autotestes de Covid-19. Para que a comercialização seja iniciada, as empresas interessadas precisam antes pedir o registro junto à Anvisa. Por isso, a medida não tem efeito imediato, cada solicitação será analisada. Os autotestes liberados são os de antígenos - feitos a partir da coleta do material no fundo da boca e do nariz e busca sinais de anticorpos ativos, gerados pelo corpo após a infecção. Os testes RT-PCR é mais preciso e detecta a presença do material genético do coronavírus. O Ministério da Saúde deve incluir as orientações da Anvisa sobre o uso de autotestes no Plano Nacional de Expansão de Testagem para Covid-19 (PNE Teste). A Anvisa também sugeriu que as empresas criem estratégias para que as pessoas que realizem os testes e tenham resultado positivo possam informar os resultados de forma online. A estratégia é evitar uma subnotificação. Além disso, resutados positivos em autoteste não necessariamente confirmam infecção por Covid-19. Assim, é preciso procurar uma unidade de atendimento para realizar a confirmação do diagnóstico, considerou a Anvisa.
Área técnica da Anvisa recomenda o uso da Coronavac em crianças de 6 a 17 anos
O pedido original do Butantan previa que o imunizante poderia ser usada em crianças a partir dos 3 anos de idade
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Divulgação | Sesab
- A área técnica da Agência Nacional de Vigilância Sanitária (Anvisa) recomendou, nesta quinta-feira (20), que o uso da Coronavac seja feito em crianças de 6 a 17 anos. O pedido original do Butantan previa que o imunizante poderia ser usada em crianças a partir dos 3 anos de idade. Outra recomendação da agência foi de que a vacina não seja aplicada em crianças imunocomprometidas. Com relação à posologia aplicada, seria a mesma dosagem que os adultos recebem e no mesmo período de tempo, com intervalo entre 2 a 4 semanas entre a primeira dose e a segunda. A versão pediátrica da vacina da Pfizer funciona de maneira diferente, com uma posologia menor. A aprovação ou não do imunizante para crianças depende da votação da Diretoria Colegiada do órgão, que ainda está em andamento. Em Salvador, o prefeito Bruno Reis e o secretário municipal de Saúde Leo Prates já deram declarações em que afirmam que, caso aprovada, a Coronavac será a escolha principal para vacinação de crianças contra a Covid-19. Nesta sexta, inclusive, o prefeito voltou a torcer pela aprovação do imunizante.
Para liberar Coronavac em crianças, Anvisa pede informações a Butantan
Atualmente, apenas o imunizante da Pfizer foi autorizado para o público infantil
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) solicitou informações complementares para analisar o pedido de uso emergencial da Coronavac no público infantil. A decisão foi tomada nesta terça-feira (21) após reunião com técnicos da Anvisa, representantes do Instituto Butantan e sociedades médicas. De acordo com a análise feita pelos pesquisadores da Anvisa e especialistas, como pediatras e imunologistas, os dados apresentados pelo instituto paulista não são suficientes. Os avaliadores entenderam que o Butantan precisa apresentar dados ''ausentes no processo'' para, depois, avaliar se libera ou não a vacina da Coronavac em crianças e adolescentes. ''A Anvisa vai encaminhar ao Instituto uma série de questionamentos sobre dados que ainda não estão presentes no processo e que impedem a conclusão da análise pela Agência'', informou a agência reguladora em nota. A reunião foi divida em duas etapas. Primeiro os representantes do Instituto apresentaram estudos sobre o imunizante em crianças e passaram a responder aos questionamentos de especialistas presentes no encontro. Na segunda etapa, apenas técnicos da reguladora e representantes de sociedades médicas analisaram as informações prestadas pelo Butantan. ''Na avaliação dos técnicos da Anvisa e dos especialistas externos convidados há lacunas importantes nos dados apresentados pelo Butantan que ainda impedem afirmar de forma científica o grau de imunidade gerado nas crianças e adolescentes.'' O Instituto Butantan divulgou uma nota em que ''agradece as associações médicas'' que estiveram na reunião e informou que ''foram apresentados dados robustos sobre imunogenicidade e segurança do imunizante mostrando, mais uma vez, que há elementos suficientes para autorização''. Por se tratar de vacinas para crianças, a Anvisa incluiu as reuniões com especialistas da área no processo de autorização de imunizantes para esse público. Segundo a agência, a mesma medida foi adotada durante os estudos sobre a vacina da Pfizer, liberada para crianças na semana passada.
Anvisa aprova novo tratamento para HIV
Medicamento aprovado reúne dois antirretrovirais em uma dose
Por: Kamille Martinho
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução
- A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou um novo medicamento para o tratamento do HIV. Trata-se da combinação de duas substâncias – a lamivudina e o dolutegravir sódico – em um único comprimido. Para a agência, a aprovação representa um avanço no tratamento, já que reúne em uma dose diária dois antirretrovirais. “A possibilidade de doses únicas simplifica o tratamento e a adesão de pacientes”, informou, por meio de nota. De acordo com a bula aprovada pela Anvisa, o novo medicamento reduz a quantidade de HIV no organismo, mantendo-a em um nível considerado baixo. Além disso, o remédio promove o aumento da contagem de cédulas CD4, que exercem papel importante na manutenção de um sistema imune saudável, ajudando a combater infecções. Indicação - O novo medicamento será indicado como um regime complemento para o tratamento da infecção pelo vírus da imunodeficiência humana tipo 1 (HIV-1) em adultos e adolescentes acima de 12 anos pesando pelo menos 40 quilos, sem histórico de tratamento antirretroviral prévio ou em substituição ao regime antirretroviral atual em pessoas com supressão virológica. O registro foi concedido ao laboratório GlaxoSmithKline Brasil Ltda. que, segundo a Anvisa, apresentou estudos de eficácia e segurança com dados que sustentam as indicações autorizadas. A bula aprovada pode ser consultada aqui.
Mais de 4 mil baianos tomaram vacinas interditadas pela Anvisa
Órgão de vigilância identificou irregularidades no envase dos imunizantes
Por: Juliana Rodrigues
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- Cerca de 4 mil baianos receberam doses de Coronavac provenientes de lotes interditados pela Agência Nacional de Vigilância Sanitária (Anvisa). O órgão de vigilância identificou irregularidades no envase dos imunizantes. De acordo com a Secretaria de Saúde do Estado da Bahia (Sesab), 4.161 pessoas receberam doses de lotes que estão proibidos de serem utilizados. A pasta ainda não concluiu um levantamento de quantas e quais prefeituras imunizaram baianos com as doses e está oficiando os municípios que receberam os lotes interditados para fazerem a devolução.No total, a Bahia recebeu 575.980? doses da vacina interditada, sendo 571.280 em 1º de setembro e 4.700 em 27 de julho. Estão inclusos nas restrições lotes 202107101H, 202107102H e L202106038. É possível conferir no seu cartão de vacinação ou na plataforma do Conecte SUS quem recebeu imunizantes destes lotes. Das vacinas recebidas na Bahia, 234.380? foram entregues a 294 municípios. Todos já foram comunicados para interromper a vacinação dos lotes específicos. Em todo Brasil, o Ministério da Saúde distribuiu 25 lotes de 42 que estão comprometidos. No total, são 12 milhões de doses que foram distribuídas no país e não puderam ser utilizadas. O Instituto Butantan afirma que as doses irregulares têm segurança e qualidade.
Anvisa aprova uso emergencial do regdanvimabe, remédio para tratamento da Covid
Por: Luciane Freire
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)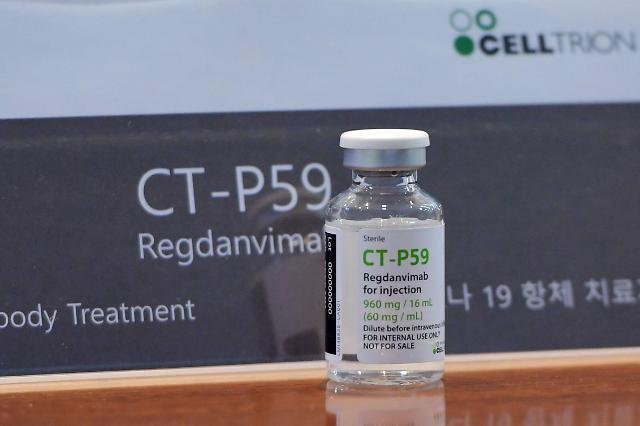
Foto: Reprodução | Getty Images
- A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta quarta (11) o uso emergencial do medicamento regdanvimabe para o tratamento da Covid-19. Trata-se de um anticorpo para o tratamento de casos leves a moderados em pacientes adultos que não necessitam de suplementação de oxigênio. O medicamento passou por unanimidade no crivo da agência. De acordo com a gerência-geral de medicamentos da agência, "o regdanvimabe deve ser administrado assim que possível após teste viral positivo para Sars-CoV-2 e dentro de 7 dias após o início dos sintomas”. Isso porque fármacos do tipo podem colaborar com a piora do quadro clínico de pacientes que necessitam de suplementação de oxigênio de alto fluxo ou ventilação mecânica, informou o Gustavo Mendes, gerente do departamento. Ele disse que o medicamento seria como uma “prevenção” para o agravamento da doença. O uso deverá ser direcionado a pacientes com fatores de alto risco para a evolução do quadro da doença.
Governador da Bahia diz que pode abrir mão da Sputnik V após impasse com Anvisa
Aceleração da vacinação e falta de autorização da Anvisa tiram a importância da compra do imunizante russo
Por: Rodrigo Meneses
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Marcos Oliveira | Sudoeste Bahia
- A demora para obter a autorização junto a Anvisa (Agência Nacional de Vigilância Sanitária) para poder importar a vacina Sputnik V pode inviabilizar a compra do imunizante russo pelo Consórcio Nordeste. O governador Rui Costa (PT) disse durante o Papo Correria que irá se reunir, ainda esta semana, com os governadores do Consórcio Nordeste para tomar uma decisão sobre a compra. Com o avanço da vacinação, a compra da vacina russa perdeu importância. Além disso, o ministro da Saúde Marcelo Queiroga declarou recentemente que o Brasil não precisa da Sputnik. “Caso a Anvisa e o Ministério da Saúde continuar colocando barreiras, não faz sentido comprar a Sputnik. Compramos no primeiro semestre”, disse Rui. "Faremos uma nova reunião essa semana. Conversei com o presidente do Consórcio Nordeste essa semana para tomar uma decisão, dada os sucessivos obstáculos da Anvisa e a própria declaração do ministro”, completou Rui. O governador esclareceu que nenhum valor foi pago para a empresa russa, porque a condição de pagamento no contrato é a entrega da vacina juntamente com a autorização da Anvisa, coisas que ainda não aconteceram.
Consórcio Nordeste assina termo com Anvisa para importação da Sputnik V
Expectativa é receber inicialmente pouco mais de 1 milhão de doses do imunizante russo
Por: Kamille Martinho
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | GOV/BA
- Os governadores dos estados do Nordeste assinaram nesta quinta-feira (8) o termo de compromisso com a Agência Nacional de Vigilância Sanitária (Anvisa que autoriza a importação e uso emergencial da vacina Sputnik V. O documento exige que as gestões monitorem a população que receberá o imunizante russo e notifiquem a agência em caso de algum evento adverso. Segundo a Anvisasomente após a assinatura deste termo é que será possível protocolar o pedido de importação para o Brasil. Presidente do Consórcio Nordeste, o governador do Piauí, Wellington Dias (PT), diz que o objetivo é agora acertar a data para a entrega de 1 milhão e 147 mil doses. "Essas doses, elas vão passar por um critério de primeira e segunda dose, acompanhado, exatamente monitorado como está no termo, termo que estamos aqui celebrando com a Anvisa”, afirmou. Quando a Anvisa aprovou a importação controlada da Sputnik V, no dia 4 de junho, a autorização foi dada com uma série de restrições. A agência impôs cerca de 30 condicionantes para a vacina desembarcar em solo brasileiro, entre elas a assinatura do Termo de Compromisso e que a Anvisa não recomenda a aplicação do imunizante russo em grávidas, pessoas com doenças não controladas, com HIV e com histórico de anafilaxia pós-vacinação. Os lotes a serem destinados ao Brasil devem ser provenientes das fábricas inspecionadas pelos técnicos da agência na Rússia e fica autorizada a importação excepcional e temporária correspondente a doses para vacinação de 1% da população de cada um dos estados que compraram o imunizante.
Anvisa autoriza testes para nova vacina contra a covid-19
Ensaio clínico terá participação de 150 voluntários brasileiros; Bahia está entre os estados onde haverá recrutamento
Por: Luciane Freire
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a realização de testes clínicos no Brasil para uma nova vacina de combate à Covid-19, do laboratório Sanofi Pasteur, com sedes na França e nos Estados Unidos. Os testes da vacina da Sanofi Pasteur devem contar com a participação de 150 voluntários brasileiros nos estados da Bahia, Minas Gerais, Mato Grosso do Sul e Rio de Janeiro. O ensaio clínico autorizado será de fase ½, quando a vacina é aplicada inicialmente em grupos pequenos de adultos saudáveis e depois em grupos que representam a população alvo que se pretende imunizar. Nos ensaios da Sanofi Pasteur, serão testadas dosagens diferentes para empregar na Fase 3. É nesse momento que o imunizante é testado em um número maior de pessoas, com vistas a avaliar eficácia e segurança. A tecnologia empregada do imunizante é a de RNA mensageiro. Além do Brasil, os ensaios deverão ocorrer nos Estados Unidos, em Honduras e na Austrália. Segundo a Anvisa, este é o nono estudo autorizado pela agência para imunizantes contra a Covid-19. Foram autorizados testes semelhantes para as vacinas da Pfizer, AstraZeneca, CoronaVac, Janssen, Clover, Medicago e Covaxin.
Anvisa autoriza estudo sobre dose de reforço da vacina Pfizer
Farmacêutica vai avaliar segurança e capacidade da resposta imune do fármaco
Por: Luciane Freire
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou hoje um estudo clínico para testar uma dose de reforço da vacina da Pfizer em pessoas que já foram vacinadas com as duas primeiras doses. Os testes clínicos serão feitos nas cidades de Salvador e São Paulo. Segundo a agência, qualquer pessoa com mais de 16 anos que tenha recebido as duas doses do imunizante produzido pela farmacêutica há pelo menos seis meses poderá ser incluído na pesquisa. O estudo pretende recrutar 443 participantes no centro clínico do Hospital Santo Antônio da Associação Obras Sociais Irmã Dulce, na capital baiana, e 442 participantes no Cepic (Centro Paulista de Investigação Clínica e Serviços Médicos), na capital paulista.
Anvisa aguarda documentos do Butantan para estudo sobre a Butanvac
Instituto se comprometeu a fornecer os dados faltantes até amanhã (07)
Por: Luciane Freire
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) informou hoje (6) que aguarda documentos do Instituto Butantan para avaliar o pedido de início de estudos com seres humanos para o desenvolvimento da vacina brasileira, Butanvac. De acordo com a Anvisa, este momento em que são necessárias informações complementares constituem a fase do processo se que o órgão chama de “exigência”. Os últimos dados recebidos foram sobre o protocolo clínico, que estão sendo analisados pela equipe técnica da Agência. Ainda segundo a o órgão, o Instituto Butantan se comprometeu a fornecer os dados faltantes até amanhã (7).
Rui celebra liberação da Sputnik V, mas lamenta limitação de doses: "Muito abaixo da necessidade"
Agência autorizou que estado use, de forma excepcional e temporária, apenas 300 mil doses do imunizante russo para aplicação na população
Por: Alexandre Santos
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)
Foto: Marcos Oliveira | Sudoeste Bahia
- O governador da Bahia, Rui Costa (PT), comemorou na noite desta sexta-feira (4) a decisão da Agência Nacional de Vigilância Sanitária (Anvisa) de autorizar, em caráter excepcional e temporário, estados do Nordeste a importar a Sputnik V, vacina russa contra o novo coronavírus. Pelo Twitter, o chefe do Executivo estadual afirmou, no entanto, estar "muito abaixo da real necessidade" a quantidade de imunizantes liberados para uso de somente 1% da população nacional — o que permitirá ao governo baiano aplicar apenas 300 mil doses das 9,7 milhões já compradas. “É apenas o início, mas depois de muita luta conseguimos aprovação para importar e aplicar a Sputnik V. A quantidade autorizada pela Anvisa está muito abaixo da real necessidade. Agora, é batalhar para fazer chegar logo o que foi aprovado e vacinar nosso povo. Vacina salva vidas”, escreveu o governador no Twitter. Assinado em março, o acordo para a aquisição da Sputnik V faz parte de uma negociação do Consórcio Nordeste com o Fundo de Investimentos Diretos da Rússia, que fornecerá o total 37 milhões de doses ao Brasil. No dia 26 de abril, a Anvisa rejeitou, por unanimidade, a importação e o uso do fármaco russo pelo Brasil. Um dos técnicos do órgão apontou “falta de documentação” e possíveis riscos do imunizante à saúde, dentre os quais a presença ou não de adenovírus com capacidade de replicação no corpo dos pacientes que receberem doses da vacina.
Importação da Sputnik V acaba de ser aprovada pela Anvisa, anuncia secretário de Saúde da Bahia
Por: Redação do Sudoeste Bahia
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)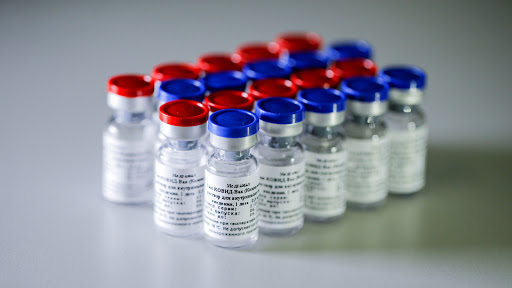
Foto: Divulgação | Gov/BA
- Por meio do Twitter, o secretário estadual de Saúde, Fábio Villas-Boas, acaba de anunciar que a vacina russa Sputnik V foi aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa), para importação excepcional. Segundo Fábio, o voto do relator Alex Campos deverá ser seguido pelos demais. Vilas-Boas celebrou a aprovação, e afirmou que a vacina irá ajudar a salvar a vida de milhares de pessoas. Na rede social, o chefe da pasta disse que pessoas saudáveis de 18 a 60 anos poderão tomar o imunizante. Ainda de acordo com o secretário, a vinda da Sputnik é mais uma luta vencida pelo governo Rui Costa (PT).
Com documentos mandados pela Bahia, Anvisa analisa hoje aprovação da Sputnik V
Em abril, agência negou importação emergencial de quase 30 milhões de doses da vacina russa contra Covid-19
Por: Adele Robichez
Ouvir Notícia
Narração automática (IA)Ouvindo Notícia
Narração automática (IA)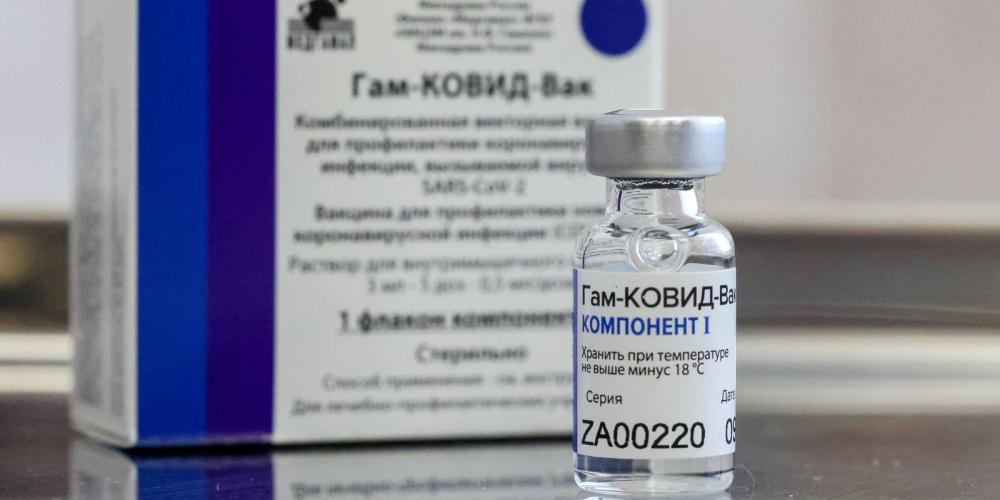
Foto: Reprodução | Agência Brasil
- A Agência Nacional de Vigilância Sanitária (Anvisa) vai analisar, na tarde desta sexta-feira (4), a nova documentação enviada pelos estados da Bahia e Maranhão, para a aprovação da vacina Sputnik V. Caso ela seja concedida, o imunizante poderá ser adicionado ao Programa Nacional de Imunização (PNI). Na primeira análise, em abril, a Anvisa negou, em decisão unânime, a importação emergencial de quase 30 milhões de doses da vacina russa contra a Covid-19, solicitada por 14 estados. De acordo com o órgão, a empresa fabricante não enviou os relatórios necessários para a análise de qualidade necessários para aprovação. Por conta disso, a compra de 9,7 milhões de doses da vacina Sputnik V, formalizada pelo Governo da Bahia, não pôde avançar. O primeiro lote com doses do imunizante chegaria ao estado no mês de abril.



























